Afinidad Electronica Del Nitrogeno
Se considera la afinidad electrónica -o electroafinidad- como el fenómeno que ocurre cuando un átomo gaseoso neutro capta un electrón y libera energía convirtiéndose en un ión negativo mononegativo. En general la afinidad electrónica aumenta hacia la izquieda y hacia arriba con las excepciones del grupo 2 y 15.
Tema 2 Estructura Electronica De Los Atomos
Al observar la tendencia periódica en la tabla los elementos aumentan su.
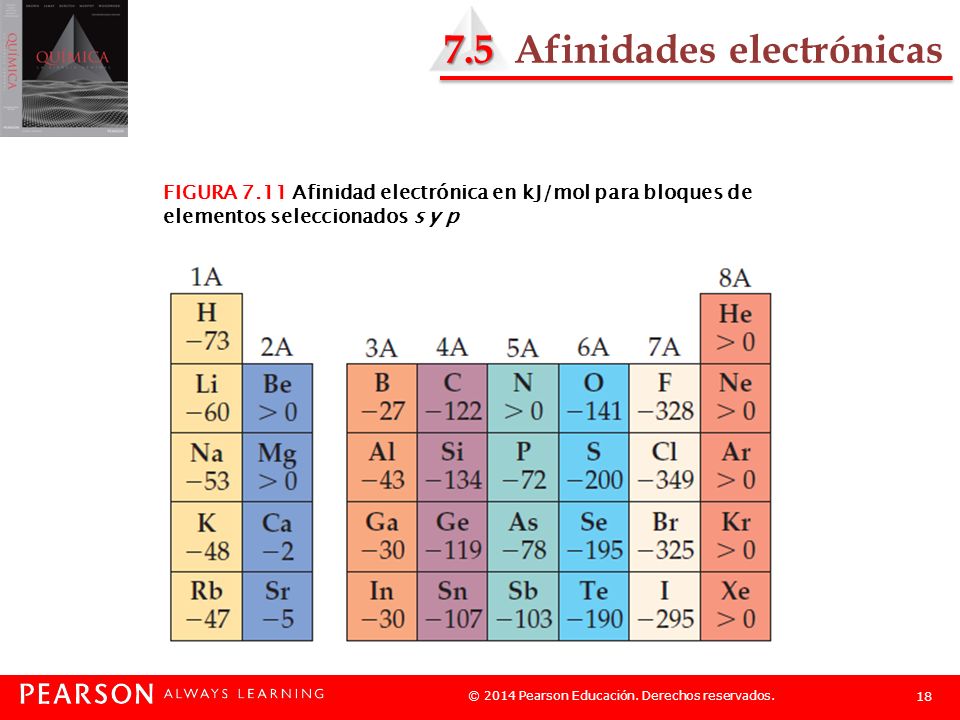
Afinidad electronica del nitrogeno. Ocurre con el resto de elementos del mismo periodo. La afinidad electrónica aumenta de izquierda a derecha en un períodoEsto se debe a que a medida que avanza un período el número de protones de los elementos aumenta y el electrón externo está protegido del núcleo en la misma medida por el mismo número de capas de electrones internas completas por lo tanto el blindaje es el mismo. Puede tomar valores n 1 2 3.
El cloro tiene mayor afinidad electrónica que el flúor. El nitrógeno tiene mayor afinidad electrónica que el boro siendo 7 y -267 repectivamente. Número cuántico principal n.
No te preocupes en este vídeo entenderás a la perfección todo sobre la afinidad electrónica con explicación. AE E0 E-Por lo tanto corresponde a la energía liberada en la reacción de. La afinidad electrónica del nitrógeno es una de las más altas superada solo por la del flúor y el oxígeno.
La afinidad electrónica del nitrógeno es de 7 kJ mol. Mira que hay temas interesantes para hablar pero bueno. El nitrógeno tiene mayor afinidad electrónica que el boro siendo 7 y -267 repectivamente.
Te cuesta entender la afinidad electrónica. En química y física atómica la afinidad electrónica de un átomo o molécula se define como. A partir del cloro la tendencia es la esperada en función de la mayor distancia de los electrones exteriores al núcleo.
Afinidad electrónica Este parámetro está relacionado con la energía del proceso de aceptación de un electrón por un átomo dado. Conviene conocer otra excepción a esta regla que encontramos en el grupo de los halógenos. Esto le sucede por ejemplo a los elementos con configuración electrónica s 2 ya que el electrón tendría que incorporarse al orbital p de mucha mayor energía como es el caso del Berilio del Magnesio o del Calcio.
La afinidad electrónica AE o electroafinidad se define como la energía involucrada cuando un átomo gaseoso neutro en su estado fundamental de mínima energía captura un electrón y forma un ion mononegativo. La primera afinidad electrónica es positiva porque se libera energía cuando un electrón se une al O o al S. Hola Amigos de la QuímicaEn el vídeo de hoy explicamos la afinidad electrónica AE.
Afinidad Electrónica positiva se absorve energía. Lo podeis ver en la siguiente imagen. Sin embargo la unión del segundo electrón requiere energía debido a la repulsión dada por la carga negativa que está presente en O-o S-.
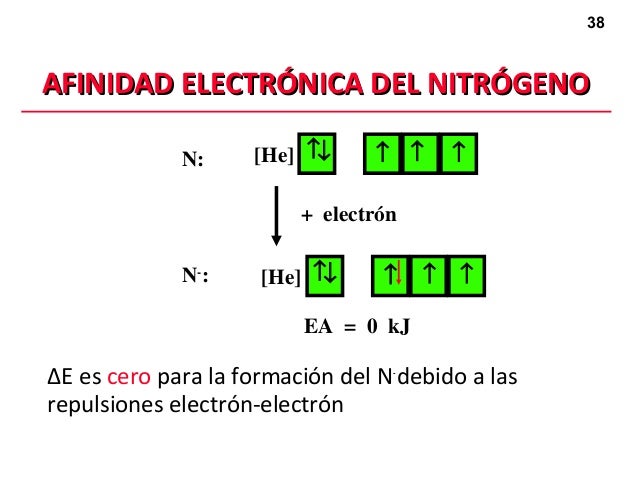
Esto significa que los nitruros son un grupo grande de compuestos que tienen un rango amplio de proporción. Se da cuando hay que proporcionar energía al átomo para captar al ion. Por qué el Nitrógeno atómico tiene una afinidad positiva y tan distinta a la de sus vecinos de la tabla periódica.
Qué poca afinidad tienen algunos. El nitrógeno tiene una afinidad electrónica muy por debajo de sus elementos vecinos tanto del periodo como de su grupo lo que es debido a su. En la Mecánica Cuántica se necesitan tres números cuánticos para describir la posición de los electrones alrededor del núcleo y un cuarto número cuántico que describe el comportamiento de un electrón.
El cambio de energía en kJ mol de un átomo o molécula neutro en la fase gaseosa cuando se agrega un electrón al átomo para formar un ion negativo. El otro día charlando con uno de vuestros compañeros surgió una cuestión. La AE es una propiedad periódica por lo que vamos a ver también como v.
Sin embargo a diferencia del radio atómico y la energía de ionización esta propiedad de los elementos químicos no tiene un comportamiento regular a lo largo de la tabla periódica ya que depende de muchos factores. Se considera la afinidad electrónica -o electroafinidad- como el fenómeno que ocurre cuando un átomo gaseoso neutro capta un electrón y libera. Entre las dificultades en el aprendizaje de las propiedades periódicas quizás el factor más importante que dificulta la compresión de la afinidad electrónica en particular es que los libros de texto no ofrecen un discurso unificado sobre esta propiedad.
Dado que se trata de energía liberada pues normalmente al insertar un electrón en un átomo predomina la fuerza atractiva del núcleo que tiene signo negativo. ESTRUCTURA ELECTRONICA DE LOS ATOMOS. La afinidad electrónica es otra propiedad periódica que nos da información sobre el comportamiento químico de los elementos.
Más allá al descender en el grupo la afinidad electrónica generalmente disminuye como se puede esperar. Un átomo del grupo16VI como O o S tienen dos vacantes en sus orbitales p de la capa de valencia y puede alojar dos electrones adicionales. Formalmente la afinidad electrónica se define como la diferencia de energías totales entre el átomo A y su ion negativo A-.
En el caso de elementos como el platino y el oro sus orbitales s contraídos ocasionan que al recibir un electrón aunque reaccionen difícilmente este sea rápidamente estabilizado.

Quimicas Ejemplos De Electronegatividad
Tema 2 Estructura Electronica De Los Atomos
Afinidad Electronica Fisicoquimica

Distribucion Electronica Del Nitrogeno Ejercicio Resuelto 4 Youtube
Propiedades Periodicas Y Configuraciones Electronicas
Que Poca Afinidad Tienen Algunos
Http Ies Fernandorios Centros Castillalamancha Es Sites Ies Fernandorios Centros Castillalamancha Es Files Descargas Tema 209 20quimica 20 282016 29 Pdf

Quimica Afinidad Electronica Excepciones Tabla Periodica Bachillerato Aulaexpress Youtube
Por Que La Afinidad Electronica Del Cloro Es Mas Que El Fluor Quora

7 5 Afinidades Electronicas La Fisica Y Quimica
Tema 2 Estructura Electronica De Los Atomos
Tema 2 Estructura Electronica De Los Atomos
Http Ies Fernandorios Centros Castillalamancha Es Sites Ies Fernandorios Centros Castillalamancha Es Files Descargas Tema 209 20quimica 20 282016 29 Pdf
Tema 2 Estructura Electronica De Los Atomos







Posting Komentar untuk "Afinidad Electronica Del Nitrogeno"